Hay temas en la biología humana que suenan ordinarios hasta que alguien los mira con detenimiento y descubre que bajo esa superficie aparentemente humilde se esconden funciones fascinantes, misterios evolutivos y debates científicos que atraviesan generaciones. El apéndice, esa pequeña prolongación en forma de dedo adherida al ciego del intestino grueso, es uno de esos temas. Durante décadas fue tratado por muchos como un órgano vestigial, un resto sin importancia evolutiva cuya única notoriedad era su propensión a inflamarse. Sin embargo, en las últimas décadas el foco se ha desplazado hacia otra dimensión del apéndice: su denso y activo tejido linfoide. En este artículo conversacional voy a llevarte por un viaje que empieza en la anatomía y llega hasta las implicaciones inmunológicas, microbiológicas y clínicas del tejido linfoide apendicular, con historias, metáforas y datos para que entiendas por qué ese pequeño órgano merece mucha más atención de la que le dimos en la escuela.
Al abordar la función del tejido linfoide en el apéndice no sólo hablamos de células y anticuerpos, sino también de cómo el cuerpo mantiene una relación sofisticada con el mundo microbiano que lo habita, de cómo se desarrollan las defensas en edades tempranas y de por qué la pérdida de una estructura no siempre equivale a la pérdida de una función. A lo largo de este texto, procuraremos balancear la explicación científica con ejemplos prácticos y reflexiones sobre lo que todo esto significa para la salud humana, la medicina y la investigación. Te invito a leer con atención y a permitirte sorprender por la complejidad y la belleza de un órgano que, aunque pequeño, juega un papel que podría considerarse estratégico en la inmunidad intestinal.
Antes de entrar en detalles técnicos, quiero que te quedes con una idea clave que guiará todo lo demás: el tejido linfoide del apéndice no es un agregado aleatorio de células; es una estructura organizada y dinámica que interacciona con la mucosa intestinal y la microbiota para contribuir a la defensa, la tolerancia y la memoria inmunitaria. Desde allí veremos cómo se organiza, qué tipos celulares lo componen, qué evidencia existe sobre sus funciones concretas y cómo su papel se integra en el panorama general del sistema inmunitario humano.
Anatomía e histología del apéndice: más que un simple tubo
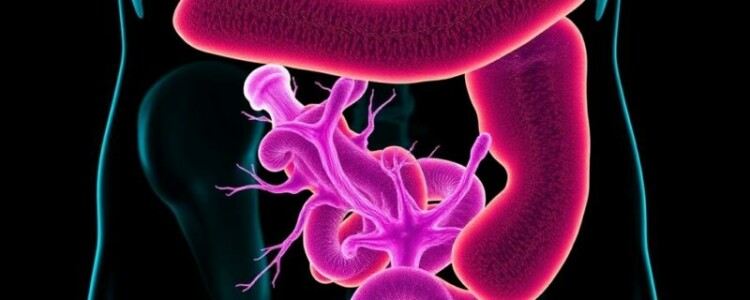
Cuando pensamos en anatomía del apéndice, lo visualizamos como una pequeña bolsa tubular unida al ciego, típicamente localizada en la región inferior derecha del abdomen. Esa descripción externa es correcta, pero lo que realmente interesa aquí es su interior: la mucosa del apéndice contiene abundante tejido linfoide organizado en folículos que recuerdan a las placas de Peyer del intestino delgado. Estos folículos no están distribuidos de forma azarosa; suelen formar anillos y agrupaciones que varían según la edad y la exposición antigénica. En niños y jóvenes el órgano presenta una mayor densidad de folículos linfoides y centros germinales activos, lo que sugiere un papel particularmente relevante en las etapas tempranas de la vida donde se está construyendo el panorama de la inmunidad mucosal.
Si miramos al apéndice a nivel micro, encontramos una mucosa con epitelio columnar, una lámina propia rica en células inmunitarias y una submucosa donde se localizan gran parte de los folículos linfoides. Entre las estructuras celulares destacan linfocitos B en los folículos, linfocitos T en zonas interfoliculares y células presentadoras de antígeno, como las células dendríticas. Además, existen células de la inmunidad innata, incluidas células linfoides innatas (ILCs), macrófagos y neutrófilos en situaciones de activación. La presencia de células M (microfold) en la región epitelial facilita la captación de antígenos luminales y su transferencia a las células del tejido linfoide, desencadenando respuestas adaptativas cuando procede.
Es importante mencionar que la vascularización y el drenaje linfático del apéndice permiten la comunicación bidireccional con los ganglios mesentéricos y con la circulación sanguínea. Este tejido linfoide no está aislado: es parte de la extensa red del sistema inmunitario mucoso —la GALT (gut-associated lymphoid tissue)— que coordina respuesta y tolerancia en un entorno lleno de microbios y antígenos alimentarios. Entender esta conectividad funcional es clave para comprender cómo las señales que nacen en el apéndice pueden tener efectos locales y sistémicos.
Desarrollo del tejido linfoide apendicular
El desarrollo del tejido linfoide en el apéndice comienza en la vida fetal y continúa con fuerza en los primeros años. La exposición temprana a antígenos ambientales y microbiota modula la maduración de los folículos y la formación de centros germinales. En términos de ontogenia inmunológica, el apéndice funciona como una “escuela” donde el sistema inmune aprende a diferenciar entre microbios beneficiosos y potencialmente dañinos, favoreciendo la generación de linfocitos B productores de IgA secretora, cruciales para la inmunidad de la mucosa.
Durante la infancia hay una marcada plasticidad: las interacciones entre epitelio, células dendríticas y linfocitos modelan la composición celular del órgano. Con la edad, y en ausencia de estímulos antigénicos intensos, la densidad linfoide puede disminuir, aunque sigue existiendo una base funcional que mantiene la capacidad de respuesta. Esta evolución ontogenética explica por qué el apéndice inflamado es más frecuente en ciertos rangos etarios y ayuda a contextualizar su papel en la inmunidad a lo largo de la vida.
El tejido linfoide: ¿qué es y cómo funciona?
El término «tejido linfoide» engloba poblaciones celulares especializadas y una arquitectura que permite el reconocimiento de antígenos, la activación de linfocitos y la producción de anticuerpos. En el apéndice, como en otros sitios de tejido linfoide asociado a mucosas, se reúnen células B y T organizadas en folículos y paracorticales, donde se producen interacciones esenciales: las células presentadoras de antígeno presentan fragmentos microbianos a linfocitos T; los linfocitos T de ayuda activan a los linfocitos B; y en los centros germinales, los B sufren expansión clonal, selección y maduración para producir anticuerpos de alta afinidad, predominantemente IgA en el contexto mucoso.
Además de las interacciones adaptativas, el tejido linfoide apendicular alberga mecanismos innatos que actúan como primera línea de defensa. Células epiteliales en comunicación con el sistema inmune sintetizan péptidos antimicrobianos y quimiocinas; las células dendríticas y macrófagos filtran y procesan antígenos; y las ILC2 o ILC3 pueden modular la respuesta inflamatoria y la homeostasis tisular. Esta mezcla de respuestas innatas y adaptativas convierte al apéndice en un microcentro inmunológico capaz de modular la composición microbiana y las reacciones a patógenos.
Otra función clave a destacar es la producción de linfocitos B productores de IgA. La IgA secretora actúa sobre la mucosa neutralizando patógenos sin provocar una inflamación destructiva, lo que permite coexistencia con microbiota beneficiosa. La generación y secreción de IgA en la luz intestinal contribuye a la barrera funcional de la mucosa y a la regulación fina del ecosistema microbiano intestinal.
Células y moléculas clave del tejido linfoide apendicular
Para entender mejor la maquinaria, aquí tienes una lista de componentes esenciales: células B (incluidos centros germinales), linfocitos T CD4+ y CD8+, células T reguladoras (Treg), células dendríticas, macrófagos, células linfoides innatas, células M en el epitelio y epitelio secretor de péptidos antimicrobianos. Cada una de estas poblaciones cumple roles concretos: desde la captura y presentación de antígenos hasta la regulación de la inflamación y la producción de anticuerpos. Además, moléculas como las quimiocinas, citocinas (por ejemplo IL-10, IL-17, TGF-β) y receptores de superficie dirigen el tráfico celular y la diferenciación dentro del tejido.
En resumen, el tejido linfoide apendicular es un ecosistema celular dinámico donde convergen señales que promueven la defensa efectiva y la tolerancia. Este equilibrio entre alerta y calma es esencial para que el intestino funcione correctamente sin caer en inflamación crónica, y el apéndice contribuye activamente a ese equilibrio en muchas circunstancias.
El apéndice y la inmunidad intestinal: funciones propuestas y evidencia
Con el andamiaje histológico y celular explicado, la pregunta natural es: ¿qué funciones concretas realiza el tejido linfoide del apéndice? Los expertos han propuesto varias funciones, que no son mutuamente excluyentes y que probablemente se solapan. Entre las más citadas están: (1) servir como sitio para la generación de respuestas IgA y maduración de linfocitos B, (2) actuar como reservorio de microbiota beneficiosa que repuebla el colon tras perturbaciones, (3) contribuir a la educación inmunitaria en la infancia favoreciendo tolerancia y defensa, y (4) participar en la regulación de respuestas inflamatorias locales para prevenir daño excesivo. La evidencia a favor de estas funciones proviene de estudios histológicos, experimentos en animales, observaciones clínicas y análisis microbiológicos modernos.
Por ejemplo, estudios en modelos animales han mostrado que tejidos linfoides apendiculares o estructuras análogas contribuyen a la recuperación de la microbiota tras episodios de diarrea. La idea es que el apéndice albergue una biopelícula protectora poblada por bacterias comensales resilientes que puede servir de semilla para recolonizar el colon. En humanos, estudios de microbioma comparativos han señalado diferencias en la composición microbiana de individuos con apéndice intacto versus apendicectomizados, aunque la interpretación no es directa y depende de muchos factores como edad, dieta y uso de antibióticos.
En términos inmunológicos, la presencia de centros germinales y la actividad de linfocitos B productivos de IgA en el apéndice respaldan su rol como fábrica de anticuerpos mucosos. La IgA producida ayuda a neutralizar patógenos y a modular la adherencia de bacterias a la mucosa, sin provocar inflamación excesiva. Esto es crucial para mantener una microbiota equilibrada y prevenir respuestas inmunes desproporcionadas que puedan conducir a enfermedad inflamatoria intestinal o patología sistémica.
Tabla: Células del tejido linfoide apendicular y sus funciones
| Tipo celular | Función principal | Localización | Importancia clínica |
|---|---|---|---|
| Linfocitos B | Generación de anticuerpos (IgA) y memoria humoral | Folículos y centros germinales | Defensa mucosa; su déficit puede reducir IgA secretora |
| Linfocitos T CD4+ | Ayuda a B, regulación de respuesta inmunitaria | Zonas interfoliculares | Cruciales para coordinación de respuestas; disfunción puede favorecer inflamación |
| Células dendríticas | Captura y presentación de antígeno; activación de linfocitos | Lámina propia y submucosa | Determinantes en la tolerancia vs activación |
| Macrófagos | Fagocitosis, regulación inflamatoria | Lámina propia | Modulan inflamación; relacionados con resolución o cronicidad |
| Células linfoides innatas (ILCs) | Regulación de la homeostasis mucosa y respuesta inflamatoria | Submucosa y lámina propia | Influencia en enfermedades inflamatorias y defensa frente a patógenos |
| Células M | Transporte de antígenos al tejido linfoide | Epitelio folicular | Facilitan la inducción de respuestas locales |
Interacción entre apéndice, tejido linfoide y microbiota
Una de las historias más cautivadoras del apéndice moderno es su relación simbiótica con la microbiota intestinal. En la última década, la investigación en microbioma ha proporcionado evidencias que apoyan la idea de que el apéndice puede funcionar como una cámara de seguridad microbiana: un refugio donde las comunidades bacterianas beneficiosas pueden persistir durante periodos en que la luz intestinal se vuelve inhóspita —por ejemplo, tras gastroenteritis, uso prolongado de antibióticos o diarrea intensa— y desde ahí repoblar el colon cuando las condiciones mejoran. Esta hipótesis no implica que el apéndice sea imprescindible para la recuperación microbiana en todos los casos, pero sí sugiere una función de resiliencia ecológica.
La interacción entre tejido linfoide y microbiota también se da a nivel molecular. La IgA secretora, producida en gran parte gracias a la actividad de los folículos apendiculares, actúa moldeando la comunidad bacteriana al favorecer la adherencia y la coexistencia de determinadas especies beneficiosas y al limitar la colonización por patógenos. Asimismo, las señales inmunitarias emitidas por el tejido linfoide moderan la producción de mucinas y péptidos antimicrobianos, influyendo en el nicho ecológico microbiano. Es un diálogo constante: los microbios educan al sistema inmune y, a su vez, el sistema inmune regula qué microbios prosperan y cómo lo hacen.
Este diálogo tiene implicaciones prácticas. Por ejemplo, la pérdida del apéndice podría modificar la estabilidad de la comunidad microbiana en ciertas situaciones, y aunque muchas personas viven sin él sin consecuencias aparentes, en la población a gran escala podrían existir sutiles cambios en la susceptibilidad a infecciones o en la respuesta a perturbaciones microbianas. La investigación contemporánea intenta cuantificar y clarificar estas asociaciones con técnicas de secuenciación y estudios longitudinales.
Listas: funciones derivadas de la interacción apéndice-microbiota
- Reservorio microbiano para repoblación post-infecciosa.
- Modulación de la composición bacteriana mediante IgA secretora.
- Educación inmunitaria temprana que favorece tolerancia y defensa.
- Regulación de la respuesta inflamatoria intestinal para evitar daño colónico.
- Contribución a la resiliencia ecológica del ecosistema intestinal.
Implicaciones clínicas: apendicitis, apendicectomía y salud a largo plazo
El tema clínico más conocido asociado al apéndice es la apendicitis aguda, una inflamación que puede llevar a perforación y a peritonitis si no se trata. Tradicionalmente, la apendicectomía ha sido la solución estándar. Sin embargo, la comprensión del papel inmunológico del apéndice ha suscitado preguntas sobre las consecuencias a largo plazo de extirparlo, especialmente cuando la cirugía es electiva o en contextos donde la apendicitis podría resolverse con manejo conservador en algunos casos.
Estudios epidemiológicos han explorado si la apendicectomía se asocia con cambios en la incidencia de enfermedades inflamatorias intestinales, infecciones gastrointestinales o alteraciones en el microbioma. Los resultados no son concluyentes: algunos trabajos sugieren un aumento del riesgo relativo de ciertas condiciones, mientras que otros no muestran asociación significativa. Es importante recordar que la mayoría de las personas sin apéndice gozan de buena salud y que cuando la apendicitis es franca y complicada, la extracción quirúrgica es a menudo la opción más segura. No obstante, estos hallazgos subrayan la necesidad de decisiones clínicas individualizadas y de más investigación sobre efectos a largo plazo.
Además, en ámbitos pediátricos la función inmunológica del apéndice —especialmente en la formación de IgA y la educación inmunitaria— puede tener especial relevancia. La pregunta sobre cuándo la apendicectomía temprana podría afectar a la inmunidad mucosa ha llevado a debates sobre el manejo conservador en ciertas presentaciones clínicas, aunque las pautas actuales priorizan la seguridad del paciente y la resolución de la infección aguda.
Listas: consideraciones clínicas prácticas
- En apendicitis aguda complicada (perforación, absceso extenso), la apendicectomía sigue siendo fundamental por razones de seguridad.
- En apendicitis no complicada, algunos protocolos permiten manejo conservador con antibióticos en casos seleccionados, siempre con seguimiento estricto.
- La decisión de extirpar el apéndice en otros contextos (p. ej. incidentalmente) debe sopesar riesgos quirúrgicos, edad del paciente y posibles funciones inmunológicas.
- Pacientes y clínicos deben considerar que la evidencia sobre secuelas inmunológicas a largo plazo es aún incompleta.
Evolución y perspectivas históricas: ¿por qué existe el apéndice?
La visión clásica del apéndice como un remanente vestigial del ancestro herbívoro que ayudaba a digerir celulosa ha sido revisada por la biología evolutiva moderna. Si bien es cierto que algunas especies lo usan para la digestión, la persistencia del apéndice en muchos mamíferos y su variabilidad entre especies sugiere que posee funciones adaptativas, entre ellas inmunológicas. Estudios comparativos indican que la presencia de un apéndice con tejido linfoide es frecuente en especies con hábitos sociales y dietas que favorecen la transmisión microbiana, lo que reforzaría su papel en el manejo de la microbiota.
La hipótesis del apéndice como “casa de seguridad” microbiana tiene consistencia ecológica: en ambientes donde las perturbaciones intestinales son comunes, disponer de un reservorio estable puede conferir una ventaja selectiva. Desde una perspectiva evolutiva, funciones que aumentan la supervivencia y la capacidad de recuperación frente a infecciones pueden explicar la retención del órgano. Esta visión no contradice la posibilidad de que su relevancia varíe entre poblaciones y contextos; como muchas estructuras biológicas, su utilidad es sensible al entorno y a la historia de exposición a patógenos y microbios benignos.
Reflexionar sobre la evolución del apéndice nos ayuda a comprender por qué su tejido linfoide es tan rico y organizado: no es un accidente, sino el resultado de presiones selectivas que han moldeado un microórgano con funciones inmunoecológicas valiosas.
Temas abiertos en investigación evolutiva
- Variabilidad interespecífica del apéndice y correlación con hábitos alimentarios y sociales.
- Relación entre presencia de apéndice y resiliencia frente a perturbaciones microbianas en entornos naturales.
- Impacto de cambios modernos (higiene, antibióticos, dieta) en la selección de funciones apendiculares.
Investigación reciente y preguntas abiertas
La investigación contemporánea usa herramientas de secuenciación del microbioma, técnicas de imagen molecular y modelos animales para abordar preguntas que quedaron sin respuesta en generaciones anteriores. ¿Cuánto contribuye el apéndice a la producción total de IgA en el intestino humano? ¿Qué especies microbianas son realmente características del nicho apendicular y cómo se comportan tras la apendicectomía? ¿Existen subgrupos de pacientes que, por genética o por exposición, dependen más del apéndice para mantener su homeostasis intestinal? Estas interrogantes están siendo exploradas con estudios trasversales y longitudinales que integran datos clínicos, genómicos y ecológicos.
Un campo prometedor es la investigación sobre terapias que aprovechen el concepto de “reservorio” microbiano, por ejemplo mediante transplantes localizados de microbiota o estrategias que fomenten la recolonización saludable del colon tras tratamientos antimicrobianos. También se estudian las señales moleculares que regulan la formación de centros germinales en el apéndice, con implicaciones potenciales para manipular respuestas vacunales mucosas o controlar la inflamación intestinal.
Sin embargo, muchas preguntas requieren ensayos clínicos y estudios de cohorte a largo plazo para traducir hallazgos experimentales en recomendaciones prácticas. La interacción compleja entre genética del huésped, dieta, exposición a patógenos y prácticas médicas modernas hace que las conclusiones necesiten matices y evidencias robustas.
Lista: preguntas de investigación prioritarias
- ¿Cuál es la contribución cuantitativa del apéndice a la IgA secretora total del intestino?
- ¿Cómo cambia la composición microbiana intestinal a lo largo del tiempo tras la apendicectomía?
- ¿Existen factores genéticos que modulan la dependencia funcional del apéndice?
- ¿Pueden estrategias terapéuticas dirigidas al apéndice mejorar la recuperación postinfecciosa del microbioma?
- ¿Qué rol juegan las células linfoides innatas del apéndice en enfermedades inflamatorias intestinales?
Para el clínico y el curioso: cómo integrar este conocimiento
Si eres profesional de la salud, este conocimiento sobre el tejido linfoide del apéndice debe traducirse en una lectura crítica de la evidencia y en una comunicación clara con los pacientes. Explicar que el apéndice tiene funciones inmunológicas no significa que su extirpación sea siempre perjudicial; significa que, cuando es posible y seguro, es razonable considerar opciones y discutir incertidumbres. En contextos donde la apendicitis es amenazante, la prioridad es la seguridad; en otros, la discusión compartida sobre manejo conservador versus quirúrgico puede incorporar la evidencia sobre funciones del apéndice.
Si eres lector general, el mensaje es simpler y empoderador: nuestro cuerpo es una red de estructuras interconectadas y muchas veces elementos considerados “sin importancia” tienen roles sutiles pero valiosos. Comprender el apéndice como un órgano con tejido linfoide activo nos invita a apreciar la complejidad de la inmunidad mucosa y a considerar cómo estilos de vida, uso de antibióticos y decisiones médicas pueden influir en nuestro equilibrio microbiano e inmunológico a largo plazo.
Independientemente de tu trasfondo, la ciencia del apéndice nos recuerda que la investigación médica evoluciona y que prácticas que parecían inmutables pueden ser matizadas por nuevos hallazgos. La clave está en combinar pruebas científicas, juicio clínico y preferencias individuales para tomar decisiones informadas.
Conclusión
El tejido linfoide del apéndice revela que este pequeño órgano desempeña múltiples papeles en la inmunidad intestinal: desde la generación de IgA y la educación de linfocitos hasta la modulación de la microbiota y la contribución a la resiliencia ecológica del intestino; aunque muchas personas viven bien sin él, su presencia refleja una estrategia evolutiva de gestión microbiana y defensa mucosa que podría tener implicaciones en la salud y la enfermedad; entender su anatomía, células, funciones y relaciones con la microbiota nos ayuda a tomar decisiones clínicas más informadas y a plantear nuevas preguntas de investigación que podrían enriquecer la medicina del futuro.