Si te propongo un viaje que empieza en las primeras semanas después de la concepción y termina con uno de los órganos más discutidos y misteriosos del cuerpo humano —el apéndice— ¿te subirías? La embriología del tracto digestivo revela una coreografía sorprendente de pliegues, rotaciones, abultamientos y recesos que, paso a paso, crean el tubo intestinal en el que vivimos. Entre todas estas formaciones, el apéndice ha despertado curiosidad durante siglos: ¿es simplemente un resto evolutivo sin función, o guarda un papel importante en la inmunidad y en la microbiota? En este artículo te invito a recorrer, con lenguaje claro y cercano, las etapas clave del desarrollo embrionario del intestino, cómo surge el ciego y, de él, el apéndice, qué señales moleculares orientan esos eventos, qué variantes pueden presentarse y por qué todo esto importa en la clínica moderna.
La embriología no es una sucesión de hechos secos; es una narrativa dinámica donde células que no saben aún qué serán conversan mediante señales químicas, migran, proliferan y organizan tejidos. Entender esa historia nos permite comprender por qué aparecen ciertas malformaciones, por qué la apendicitis es tan frecuente y por qué el apéndice puede desempeñar papeles inmunológicos y microbianos que solo comienzan a apreciarse con técnicas modernas. Acompáñame: empezamos por el «tubo» primitivo y vamos desgranando cada paso hasta llegar al diminuto pero famoso apéndice.
Fundamentos: cómo comienza el tubo digestivo
El tubo digestivo embryológico nace de la interacción entre tres capas germinales: el endodermo, el mesodermo y el ectodermo, cada una aportando elementos clave para la formación de las diferentes partes del sistema digestivo. Aunque pueda sonar técnico, piensa en el endodermo como la plancha que formará el revestimiento interno del tubo —la mucosa—; el mesodermo visceral envuelve y formará la musculatura, el tejido conectivo y los vasos; y el ectodermo contribuye básicamente a estructuras craneales y a ciertos nervios. Estas tres capas se reorganizan mediante el plegamiento embrionario que transforma una lámina en un tubo.
Entre las semanas 3 y 4 de gestación el embrión trilaminar comienza a plegarse en los ejes lateral y cefalocaudal, lo que lleva a la formación del intestino primitivo: un tubo continuo que, por proximidad a otras estructuras embrionarias, se diferenciará en intestino anterior, medio y posterior. Cada una de estas regiones responde a señales moleculares y a gradientes de factores de transcripción (como señales Hox, FGF y Shh) que le dictan destino y forma. La precisión de estos eventos es asombrosa: pequeñas variaciones temporales o espaciales en estas señales pueden alterar la longitud, la posición o incluso la existencia de segmentos completos.
Plegamientos embrionarios y cierre del tubo
Durante el plegamiento lateral, las capas laterales del embrión se curvan hacia la línea media y se fusionan, convirtiendo la superficie dorsal en interior y formando el conducto intestinal cerrado. Este proceso no es instantáneo: requiere coordinación entre crecimiento celular, apoptosis controlada y reorganización del mesénquima. El resultado es un tubo que, en sus extremos, se comunica temporalmente con el saco vitelino por conductos (por ejemplo, el conducto onfalomesentérico o vitelino) que tendrán como destino desaparecer o persistir en ciertas anomalías, como el divertículo de Meckel.
Posteriormente, la vascularización y la inervación comienzan a establecerse: la arteria vitelina y sus ramas nutrirán el intestino medio, mientras que plexos neuronales derivados de la cresta neural colonizarán la pared intestinal. Si esas células neurales no migran correctamente, aparecen trastornos como la aganglionosis (enfermedad de Hirschsprung), que demuestran la importancia de cada actor en la obra embriológica.
Segmentación funcional: intestino anterior, medio y posterior
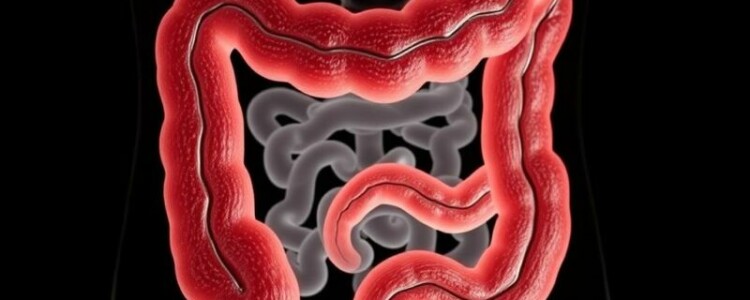
El tubo intestinal se subdivide en tres regiones con destinos distintos: el intestino anterior dará lugar al esófago, estómago, duodeno proximal, hígado y páncreas; el intestino medio formará el intestino delgado y gran parte del colon hasta el tercio proximal del colon transverso; el intestino posterior generará el resto del colon, el recto y la parte proximal del conducto anal. Esta segmentación no es meramente anatómica: cada segmento tiene patrones de vascularización, inervación y peritonealización particulares.
La porción media, donde se origina el ciego y, por ende, el apéndice, es especialmente dinámica. En la sexta semana el asa intestinal media crece de forma rápida y no cabe dentro de la cavidad abdominal aún pequeña del embrión, por lo que hernia temporalmente hacia el cordón umbilical en un proceso natural llamado herniación fisiológica. Esa herniación y su retorno posterior son fundamentales para la posición final del intestino y para la formación del ciego en su ubicación típica.
La herniación fisiológica y la rotación intestinal
Entre la sexta y la décima semana el intestino medio realiza una rotación en torno al eje formado por la arteria mesentérica superior. Primero rota 90° hacia la derecha durante la herniación, y luego, al retornarse a la cavidad abdominal, completa otros 180°, acumulando 270° en total en sentido antihorario. Este giro determina la disposición de asas, la ubicación del ciego y la dirección del mesenterio. Si la rotación falla, surgen malposiciones conocidas como malrotaciones, que pueden predisponer a vólvulos, obstrucciones o ubicaciones atípicas del apéndice.
El ciego aparece como una dilatación en la porción distal del intestino medio; su posición relativa cambia con el desarrollo y la elongación del colon, hasta situarse típicamente en la fosa ilíaca derecha. El apéndice, un divertículo en forma de tubo que surge del ciego, comienza a diferenciarse a partir de este punto inicial mediante un proceso de crecimiento diferencial: el cuerpo principal del ciego se expande más que el divertículo apendicular, lo que origina la forma típica de dedo del apéndice a lo largo del margen cecal.
Cómo surge exactamente el apéndice: del brote cecal al divertículo apendicular
El apéndice se desarrolla a partir del brote cecal, una evaginación del intestino medio que aparece alrededor de la sexta semana. En ese momento, la región cecal es una pequeña protuberancia; a medida que el intestino crece y rota, esa protuberancia va diferenciándose: la pared cecal se ensancha y el apéndice emerge como un divertículo más estrecho y alargado. La longitud del apéndice no es fija: al nacer suele ser corto, y continúa alargándose durante la infancia hasta alcanzar dimensiones adultas.
Un aspecto importante es que el lumen del apéndice experimenta cambios durante el desarrollo. Al principio el lumen está patente, pero en etapas posteriores puede producirse una obliteración transitoria por proliferación celular de la mucosa, seguida de recanalización. Este fenómeno de recanalización es conocido en varias partes del tracto digestivo embriológico y su falla parcial o completa puede explicar variantes luminales o estenosis en otros segmentos.
Señales moleculares y genes implicados
En términos moleculares, la regionalización del intestino está guiada por un conjunto de genes y señales que determinan patrónación anteroposterior y dorsoventral. Los genes Hox regulan la identidad segmentaria a lo largo del eje anteroposterior; señales como SHH (Sonic hedgehog) emanadas del endodermo influyen en el mesénquima circundante para organizar la musculatura y el estroma; factores de crecimiento como FGF y BMP modulan proliferación y diferenciación. Aunque se ha estudiado más a fondo la formación de estructuras como el estómago o páncreas, la formación del ciego y apéndice depende de la interpretación correcta de esos gradientes moleculares y de la temporización de crecimiento diferencial.
Además, la vascularización y el desarrollo del mesenterio acompañan a estas señales. La arteria mesentérica superior marca el territorio del intestino medio, y su trayectoria condiciona el pedículo mesentérico que sostiene el intestino delgado y el colon proximal. La llegada de vasos y el remodelado de los mismos ayudan a separar regiones y a orientar el crecimiento local que dará lugar al ciego y apéndice.
Histogénesis de la mucosa apendicular y tejido linfoide
Desde el punto de vista histológico, el apéndice se distingue por su abundante tejido linfoide en la submucosa y la mucosa. Este tejido linfoide comienza a poblar la pared apendicular en etapas tardías del desarrollo fetal y se incrementa significativamente después del nacimiento, durante los primeros años de vida, en relación con la exposición a antígenos microbiológicos. La mucosa apendicular comparte características con la del colon, pero su densidad de folículos linfoides es mayor, lo que sugiere un papel inmunológico particular.
La incorporación gradual de tejido linfoide y la maduración del sistema inmunitario intestinal postnatal explican por qué muchas obstrucciones apendiculares en niños se relacionan con hiperplasia linfoide: los ganglios linfoides de la mucosa se hipertróficas en respuesta a infecciones, lo que puede ocluir la luz apendicular y desencadenar apendicitis.
Una tabla con los hitos embriológicos principales
| Semana | Evento | Significado |
|---|---|---|
| 3-4 | Formación del disco trilaminar y comienzo del plegamiento | Origen del tubo digestivo y separación en capas germinales |
| 4-5 | Diferenciación en intestino anterior, medio y posterior | Determinación de destinos regionales (estómago, intestino delgado, colon) |
| 6 | Herniación fisiológica del intestino medio; aparición del brote cecal | Inicio de la formación del ciego y apéndice |
| 6-8 | Inicio del apéndice como divertículo del ciego | Formación del apéndice y establecimiento del lumen |
| 8-10 | Retorno del intestino a la cavidad abdominal y rotación final | Posicionamiento definitivo del ciego y apéndice |
| Final fetal / neonatal | Desarrollo de tejido linfoide y cambios de la mucosa | Maduración inmunológica postnatal |
Esta tabla resume pasos clave, pero recuerda que la embriología es variable: hay márgenes temporales y diferencias individuales en el crecimiento y la rotación que pueden condicionar variantes anatómicas.
Variantes anatómicas y anomalías relacionadas con el apéndice
La historia embriológica explica también por qué el apéndice puede ubicarse en diversas posiciones: retrocecal, subcecal, pélvico, intraumbilical cuando hay malrotación, e incluso en ubicaciones más raras asociadas a órganos ectópicos. La longitud del apéndice y su posición dependen de la interacción entre el crecimiento cecal, la elongación del colon y la fijación del mesenterio. En algunos individuos el apéndice puede ser muy corto o, en casos raros, estar ausente (apéndice agénico o atresia apendicular).
Entre las anomalías embriológicas que afectan al intestino medio y por ende pueden influir en la morfología apendicular están las malrotaciones intestinales, hernias congénitas, duplicaciones intestinales y persistencia del conducto vitelino (que puede dar lugar a un divertículo de Meckel —aunque éste proviene del intestino anterior medio— y suele localizarse en el íleon, no en el apéndice). Conocer estas variantes es esencial para el diagnóstico quirúrgico, porque una apendicitis atípica puede deberse a una posición inusual del órgano.
Implicaciones clínicas: por qué importa la embriología del apéndice
La embriología no es solo teoría; tiene consecuencias prácticas. La localización atípica del apéndice puede enmascarar la presentación clínica de la apendicitis, conduciendo a diagnósticos erróneos o retrasos en la intervención. Por ejemplo, un apéndice pélvico puede causar síntomas urinarios o rectales, y un apéndice retrocecal puede cursar con dolor menos localizado e irradiado a la espalda. Además, el hecho de que la hiperplasia linfoide contribuya a obstruir la luz apendicular en niños explica por qué la apendicitis pediátrica a menudo se relaciona con infecciones previas.
Desde la cirugía, la comprensión del desarrollo y la vascularización embriológica es crucial para planificar abordajes y evitar complicaciones. La base vascular y la relación del apéndice con el mesenterio influyen en la técnica de la apendicectomía, la posibilidad de hemorragias y la resección adecuada en casos de tumores apendiculares.
Listas prácticas: causas de obstrucción apendicular y factores de riesgo
- Hiperplasia linfoide de la mucosa (frecuente en niños y adolescentes tras infecciones).
- Fecalitos o concreciones fecales (más comunes en adultos).
- Tumores apendiculares (p. ej., carcinoides, adenocarcinomas raros).
- Parásitos (menos frecuentes pero posibles en áreas endémicas).
- Estrechamiento congénito o atresia parcial del lumen debida a fallos de recanalización.
Estos elementos pueden actuar como precipitados de inflamación, y su relevancia clínica se comprende mejor si se conoce la historia embrionaria del órgano y su desarrollo luminal y linfoide.
El apéndice en la evolución y en la microbiota: ¿resto inútil o reserva útil?
Durante mucho tiempo el apéndice se consideró un órgano vestigial, un resto sin función clara heredado de ancestros herbívoros que necesitaban un ciego grande para fermentar vegetación. Sin embargo, estudios comparativos y de microbioma han rescatado al apéndice como un reservorio de bacterias beneficiosas que pueden recolonizar el colon tras episodios de diarrea severa, y como un sitio de maduración y educación inmunitaria neonatal. En varias especies el apéndice presenta abundante tejido linfoide, lo que sugiere que la selección natural pudo haber conservado esa estructura por beneficios inmunológicos y ecológicos microbianos.
La evidencia no es categórica ni uniforme entre todas las especies: la presencia y la función del apéndice varían según dieta, hábitos de vida y la coevolución con la microbiota. Pero la idea de que el apéndice pudiera servir como «archivo» bacteriano cobra fuerza con estudios que muestran menor recurrencia de ciertas infecciones intestinales en personas con apéndice intacto y con observaciones evolutivas de su conservación en linajes donde resultó ventajoso.
Implicaciones para la salud pública y la cirugía
Si el apéndice contribuye a la estabilidad de la microbiota, su extirpación podría tener efectos sutiles a largo plazo en la ecología intestinal. No obstante, la apendicitis aguda es una urgencia que requiere tratamiento y muchas apendicectomías no generan secuelas significativas. La clave está en valorar riesgo-beneficio: en la era de la antibióticoterapia y la cirugía mínimamente invasiva se investiga cuándo la apendicitis no complicada puede tratarse médicamente conservadoramente, preservando potencialmente el órgano y su función microbiana. Aquí la comprensión embriológica y anatómica ayuda a identificar formas atípicas o riesgos quirúrgicos asociados a malrotaciones.
Técnicas modernas para estudiar el desarrollo intestinal
La embriología clásica se basó en cortes histológicos y observación macroscópica de embriones. Hoy contamos con herramientas poderosas: imágenes 3D, microtomografía, organoides a partir de células madre pluripotentes, trazado genético y modelos animales modificados para silenciar o activar genes específicos que nos permiten entender el papel de señales concretas en la formación del ciego y apéndice. Los organoides intestinales, por ejemplo, permiten reproducir in vitro etapas de formación de epitelio y preguntar cómo responde la mucosa a señales SHH o a la presencia de bacterias, lo que abre puertas a estudiar recanalización, proliferación y formación de tejido linfoide en condiciones controladas.
Estas técnicas no solo enriquecen la comprensión teórica: también habilitan nuevas estrategias terapéuticas, como intervenciones dirigidas a modular la microbiota o a proteger la mucosa en estadios críticos, y ayudan a explicar por qué ciertas malformaciones aparecen cuando se alteran genes clave durante ventanas temporales muy estrechas del desarrollo.
Preguntas abiertas y líneas de investigación actuales
Aunque conocemos muchos pasos del desarrollo intestinal, hay preguntas abiertas fascinantes: ¿qué determina exactamente la longitud final del apéndice en cada individuo? ¿Qué combinación de genes y señales determina la densidad de tejido linfoide apendicular y cómo varía esto entre poblaciones? ¿Cuánto contribuye la microbiota materna y la exposición postnatal temprana a la maduración apendicular? En biomedicina hay interés en si preservar el apéndice cuando es posible puede contribuir a una mejor recuperación de la microbiota tras antibióticos o gastroenteritis grave.
Además, la investigación en medicina regenerativa explora si células progenitoras del intestino pueden utilizarse para reparar segmentos dañados o reconstruir porciones del tubo digestivo. Comprender los mecanismos que rigen la formación del apéndice y la recanalización luminal aporta conocimientos potencialmente transferibles a estas áreas de innovación clínica.
Resumen clínico y puntos prácticos para estudiantes y profesionales
Para quienes tratan pacientes, recordar la embriología tiene efectos concretos: la posición del apéndice puede ser variable, la base apendicular en el ciego suele ser constante (referencia para cirujanos), la obstrucción por hiperplasia linfoide es más probable en población pediátrica, y las malrotaciones pueden generar presentaciones atípicas. En la evaluación de dolor abdominal es útil mantener en mente que el trayecto embriológico explica muchas de las variaciones anatómicas y sus consecuencias clínicas.
Una lista rápida de claves clínicas: la apendicitis pediátrica puede comenzar con dolor periumbilical y migrar; en malrotaciones el dolor puede localizarse de forma no clásica; la decisión entre tratamiento antibiótico o cirugía depende de factores clínicos, imagenológicos y de riesgo de recurrencia; y la anatomía vascular y del mesenterio debe valorarse en laparoscopias para evitar complicaciones intraoperatorias.
Tabla comparativa: características del ciego y apéndice en diferentes etapas
| Etapa | Tamaño/longitud | Tec. linfoide | Patencia del lumen |
|---|---|---|---|
| Fetal temprano (6-8 sem.) | Protuberancia cecal pequeña; apéndice como brote | Escaso inicialmente | Patente |
| Fetal tardío / neonatal | Apéndice corto, ciego más desarrollado | Comienzan a aparecer folículos linfoides | Generalmente patente; posible obliteración temporal seguida de recanalización |
| Infancia temprana | Longitud apendicular aumenta | Incremento notable por exposición microbiana | Patente |
| Edad adulta | Apéndice de longitud variable (5-12 cm típico) | Folículos linfoides bien desarrollados | Patente (salvo patologías) |
Conclusión
La embriología del tracto digestivo y la formación del apéndice son una muestra fascinante de cómo pequeños eventos celulares y moleculares construyen estructuras con repercusiones muy concretas en la salud humana; desde los pliegues que transforman una lámina en un tubo hasta la aparición del brote cecal y el lento crecimiento del apéndice, cada etapa explica variantes anatómicas, predisposiciones a la enfermedad y funciones potenciales que solo ahora empezamos a comprender en profundidad —como su papel inmunológico y microbiano—. Comprender esa historia no solo satisface la curiosidad científica, sino que orienta el diagnóstico clínico, la cirugía y nuevas líneas terapéuticas en medicina moderna.