La combinación de imágenes médicas y algoritmos inteligentes suena, para muchos, a ciencia ficción; sin embargo, hoy en día es una realidad palpable que está transformando la manera en que pensamos sobre enfermedades aparentemente sencillas, como la apendicitis. Imagine por un momento la escena en un servicio de urgencias: un paciente con dolor abdominal, incertidumbre clínica, presión para actuar rápido. La tomografía computarizada (TC) ya es una herramienta vital para decidir si ese apéndice inflama merece intervención quirúrgica. Ahora imagínele a la TC ayudada por inteligencia artificial (IA) —no para reemplazar al médico, sino para amplificar su precisión, reducir tiempos de diagnóstico y minimizar errores humanos. En este artículo desarrollaré, paso a paso y con lenguaje claro, cómo la inteligencia artificial está siendo aplicada para diagnosticar apendicitis a partir de TC, qué técnicas se emplean, cuáles son los beneficios y limitaciones reales, y qué debemos esperar en los próximos años en la integración clínica de estas tecnologías. No he recibido una lista de frases clave explícita; por tanto, integraré de manera natural términos relevantes como inteligencia artificial, apendicitis, tomografía computarizada, aprendizaje profundo y diagnóstico asistido por IA para mantener coherencia y utilidad.
¿Por qué la TC es fundamental para diagnosticar apendicitis?
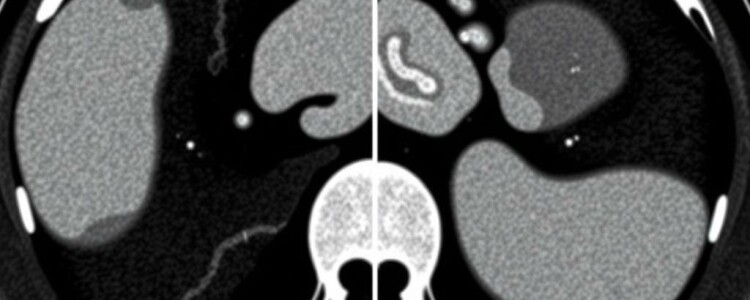
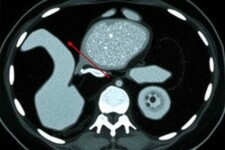
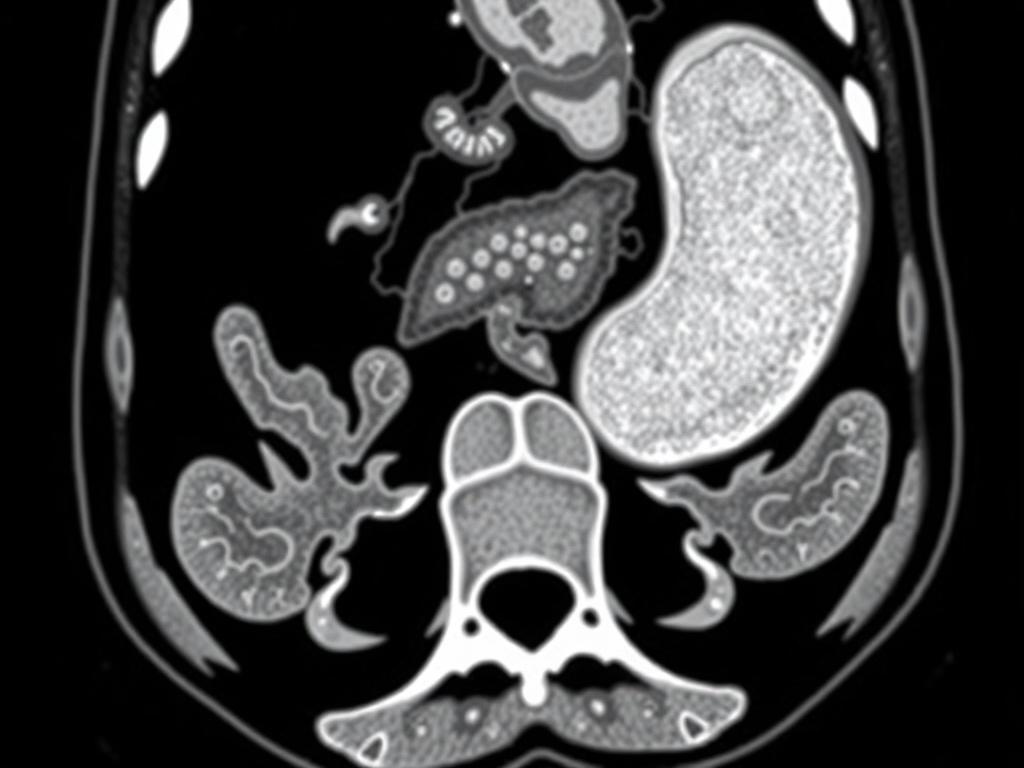
La tomografía computarizada ofrece imágenes transversales detalladas del abdomen que permiten ver el apéndice, su tamaño, la presencia de líquido, engrosamiento de la pared, y signos indirectos de inflamación o perforación. Antes de la adopción generalizada de la TC, el diagnóstico de apendicitis dependía en exceso de la exploración física, los síntomas y tablas de puntuación clínica. Eso llevaba a tasas de apendicectomías negativas (operar cuando el apéndice no está inflamado) y a retrasos diagnósticos peligrosos. Con la TC se redujo significativamente la incertidumbre, pero surgieron nuevos retos: interpretación dependiente del radiólogo, variabilidad entre observadores, y tiempos de espera en servicios saturados. Aquí es donde entra con fuerza la inteligencia artificial, no para sustituir la mirada experta, sino para estandarizar, acelerar y complementar la lectura de imágenes.
La TC es particularmente adecuada para el uso de IA porque genera datos estructurados en forma de volúmenes. Los algoritmos de aprendizaje profundo, y en especial las redes neuronales convolucionales (CNN), funcionan muy bien cuando tienen acceso a grandes cantidades de imágenes con etiquetas confiables. Cuando los modelos se entrenan con tomografías de pacientes confirmados con apendicitis y controles sin enfermedad, aprenden a detectar patrones sutiles que pueden pasar desapercibidos incluso para el ojo humano en situaciones de fatiga o carga laboral.
Ventajas clínicas de combinar TC e IA
La sinergia entre TC e inteligencia artificial promete varias ventajas concretas en la práctica clínica. En primer lugar, aumento de la sensibilidad y especificidad: los algoritmos bien entrenados pueden igualar o incluso superar a radiólogos promedio en ciertos estudios publicados, especialmente en detectar apendicitis complicada. En segundo lugar, velocidad: el procesamiento automatizado permite priorizar estudios críticos en la cola de lectura, lo que reduce tiempos hasta el diagnóstico. En tercer lugar, estandarización: las decisiones asistidas por IA pueden mitigar la variabilidad interobservador. Y en cuarto lugar, educación y apoyo: sistemas que señalan áreas de interés y proporcionan un segundo criterio ayudan a formar a residentes y jóvenes radiólogos.
No obstante, estas ventajas dependen de la calidad de los datos de entrenamiento, la validación externa y la integración correcta en el flujo de trabajo, aspectos que abordaré más adelante.
Técnicas de inteligencia artificial aplicadas a TC para apendicitis
Para entender cómo la IA hace esto, conviene conocer las técnicas más comunes y cómo se aplican concretamente al problema de la apendicitis en TC.
Redes neuronales convolucionales (CNN)
Las CNN son la columna vertebral de muchos avances en visión por computador. En el contexto de TC, las CNN 2D procesan cortes individuales, mientras que las CNN 3D procesan volúmenes completos, capturando relaciones espaciales en tres dimensiones. Para apendicitis, las CNN 3D tienden a ser más informativas porque preservan la anatomía volumétrica del apéndice y tejidos circundantes. Estas redes aprenden a distinguir tejidos inflamados, identificar colecciones y ver trayectos fistulosos sugerentes de perforación.
Segmentación y detección
Dos tareas técnicas recurrentes son la segmentación (separar el apéndice y estructuras de interés del resto de la imagen) y la detección/classificación (decidir si hay apendicitis y su probabilidad). Para segmentación se usan U-Net y variantes 3D U-Net; para detección, arquitecturas basadas en CNN clásicas o modelos de clasificación más recientes. La segmentación también ayuda a medir el diámetro del apéndice y evaluar derrames periapendiculares de forma automatizada, ofreciendo métricas cuantitativas que refuerzan la interpretación clínica.
Aprendizaje supervisado vs. no supervisado
La mayor parte de los estudios usan aprendizaje supervisado, lo que requiere imágenes etiquetadas por expertos (p. ej., radiólogos que marcan apéndices inflamados). Esto garantiza precisión al costo de tiempo y recursos. Alternativas como el aprendizaje no supervisado o auto-supervisado buscan aprovechar grandes volúmenes de imágenes sin etiquetas, reduciendo la dependencia de anotaciones manuales; sin embargo, aún están en fase de investigación para aplicaciones críticas como diagnóstico de apendicitis.
Modelos híbridos y ayudantes interpretables
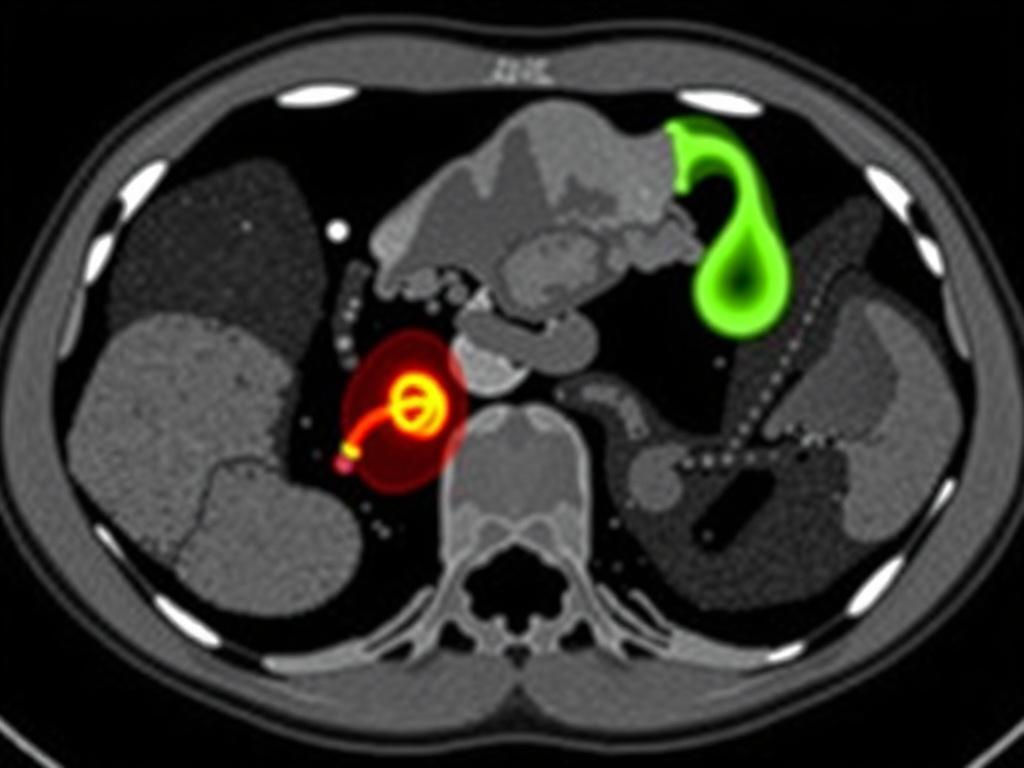
La interpretabilidad es clave en medicina. Por eso muchos sistemas combinan modelos de imagen con reglas clínicas (edad, leucocitos, signos físicos) para mejorar predicciones y ofrecer explicaciones comprensibles. Herramientas de visualización como mapas de calor (saliency maps) muestran qué regiones de la TC influyeron en la decisión del modelo, ayudando al radiólogo a confiar y validar la recomendación automática.
Ejemplos y evidencia: ¿qué muestran los estudios?
La literatura acumulada en los últimos años ofrece resultados prometedores aunque heterogéneos. Varios estudios publicados reportan que modelos de aprendizaje profundo alcanzan sensibilidades y especificidades comparables a radiólogos experimentados en cohortes internas. Otros trabajos muestran que el apoyo de IA reduce el tiempo de lectura y mejora la identificación de apendicitis complicada.
A continuación presento una tabla simplificada que resume tipos de enfoques, métricas típicas publicadas y limitaciones recurrentes:
| Tipo de enfoque | Métricas típicas | Limitaciones comunes |
|---|---|---|
| CNN 2D por cortes | Sensibilidad 0.80-0.90, Especificidad 0.75-0.88 | Pérdida de contexto 3D; dependiente de calidad de cortes |
| CNN 3D (segmentación + clasificación) | Sensibilidad 0.85-0.95, Especificidad 0.80-0.92 | Mayor demanda computacional; requiere más datos anotados |
| Modelos híbridos (imagen + clínica) | Mejora AUC en 0.03-0.07 respecto a imagen sola | Necesidad de integración de historiales y estándares de datos |
| Modelos no supervisados/auto-supervisados | Exploratorios; métricas variables | Aún experimentales para uso clínico |
Es importante enfatizar que muchas series provienen de centros específicos con protocolos de TC homogéneos; cuando esos modelos se aplican fuera de su entorno de entrenamiento, la performance puede caer. Esa es una de las razones por las que la validación externa y los estudios multicéntricos son imprescindibles.
Casos de uso prácticos
Los estudios muestran varios usos prácticos: priorizar lecturas urgentes (triage automático), ofrecer una segunda opinión en entornos con pocos radiólogos, cuantificar parámetros (diámetro del apéndice, volumen de colección), y apoyar la decisión entre manejo conservador versus quirúrgico cuando el diagnóstico es borderline. Ningún algoritmo debería dictar la conducta final sin la deliberación clínica multidisciplinaria.
Desafíos técnicos y clínicos
Aunque la promesa es grande, existen obstáculos técnicos, regulatorios y éticos que deben superarse antes de la adopción masiva.
Calidad y heterogeneidad de los datos
Los modelos son tan buenos como los datos con los que se entrenan. La variabilidad en protocolos de TC (contraste, cortes, dosis), diferencias demográficas y comorbilidades afectan el rendimiento. Además, las anotaciones humanas pueden ser inconsistentes: ¿qué define exactamente «apendicitis complicada»? La falta de definiciones estandarizadas dificulta la generalización. Por tanto, construir consorcios de datos multicéntricos con estándares de anotación es una prioridad.
Generalización y sesgos
Un algoritmo entrenado mayormente en adultos puede fallar en pediatría; uno entrenado con imágenes de alta calidad puede no manejar estudios emergentes con artefacto. Los sesgos en los datos pueden amplificar desigualdades: diagnóstico menos preciso en poblaciones subrepresentadas conduce a peores resultados.
Interpretabilidad y confianza clínica
Los médicos necesitan entender por qué un sistema sugiere apendicitis. Las «cajas negras» generan recelo. Por eso las estrategias de interpretabilidad (mapas de atención, explicaciones basadas en características) son cruciales para la aceptación clínica. Sin comprensión, la IA será vista como un cajón misterioso que podría provocar errores no entendidos.
Regulación y responsabilidad
Los sistemas de IA para diagnóstico médico requieren aprobación regulatoria (p. ej., CE, FDA u homólogos) y deben demostrar seguridad y eficacia. Además, la responsabilidad ante un diagnóstico erróneo sigue siendo un tema complejo: ¿es responsabilidad del proveedor del algoritmo, del hospital o del radiólogo que integró la recomendación a su interpretación? Las políticas legales y de seguros tienen que adaptarse.
Integración en el flujo de trabajo
Un sistema útil no es solo preciso: debe integrarse sin fricción en los sistemas de información hospitalarios (RIS/PACS, historiales electrónicos). Además, debe ofrecer resultados en tiempos compatibles con la urgencia clínica, y proporcionar interfaces que no sobrecarguen al profesional.
Implementación práctica: pasos para introducir IA en diagnóstico de apendicitis
Integrar IA en un hospital exige planificación multidisciplinaria. A continuación, un esquema paso a paso que describe un enfoque prudente y realista, sin entrar en instrucciones clínicas directas, sino centrándose en la gestión y seguridad del proceso.
- Formar un comité: incluye radiólogos, cirujanos, TI, ética y administración para evaluar necesidades y riesgos.
- Revisar evidencia: analizar estudios publicados, validaciones externas y experiencias de otros centros.
- Seleccionar solución: preferir herramientas con validación multicéntrica, explicabilidad y soporte técnico.
- Piloto controlado: desplegar en un servicio con supervisión, comparar resultados con el estándar de cuidado.
- Validación local: evaluar performance en la población del centro, ajustar umbrales y flujos de trabajo.
- Capacitación: formar a radiólogos y personal en la interpretación de salidas y limitaciones del sistema.
- Monitoreo continuo: medir performance en tiempo real, tasas de concordancia, y eventos adversos relacionados.
- Retroalimentación y mejora: actualizar modelos y procesos según hallazgos y cambios en protocolos de TC.
Este proceso protege contra despliegues prematuros y asegura que la tecnología aporte valor real sin comprometer la seguridad del paciente.
Aspectos éticos y de privacidad
El uso de IA en imágenes médicas levanta cuestiones de privacidad, consentimiento y equidad. Los datos de TC deben ser tratados con protocolos de anonimización y seguridad. Además, los pacientes deberían ser informados si un sistema automatizado formará parte de su proceso diagnóstico, especialmente cuando los algoritmos influyen en decisiones críticas.
Un punto ético complejo es la redistribución del trabajo: la IA puede mejorar eficiencia, pero también cambiar roles profesionales. Es necesario planificar la formación y el papel humano en un escenario en que las máquinas asistan, para evitar pérdida de habilidades y mantener responsabilidad clínica.
Transparencia y explicabilidad
La confianza del paciente y la sociedad depende de la transparencia: entender qué hace el algoritmo, en qué datos se basó, y cuáles son sus limitaciones. Las instituciones deben publicar métricas, procedimientos de validación y, cuando sea posible, un resumen accesible sobre el funcionamiento del sistema para audiencias no técnicas.
Impacto económico y organizacional
La adopción de IA tiene efectos directos en costos y organización hospitalaria. Por un lado, la reducción de lecturas innecesarias y la detección temprana de complicaciones pueden generar ahorros en hospitalizaciones y procedimientos evitados. Por otro lado, invertir en infraestructura, licencias, y capacitación implica gastos iniciales. Los administradores deben evaluar el retorno de inversión a medio plazo y considerar modelos de negocio sostenibles, como licencias por uso o colaboración con consorcios académicos.
Además, la IA puede cambiar la demanda de ciertos servicios: más estudios urgentes leídos rápidamente, menos derivaciones por dudas, y reasignación de tareas de interpretación rutinaria hacia actividades de mayor valor clínico y enseñanza.
Casos del mundo real y lecciones aprendidas
En centros pioneros se han observado beneficios concretos: reducción del tiempo de espera para reportes urgentes, menor variabilidad en diagnósticos iniciales y mayor detección de apendicitis complicada en pacientes con presentaciones atípicas. Sin embargo, también hay aprendizajes: muchos proyectos requerían más datos locales de los previstos, hubo necesidad de ajustar umbrales para evitar falsas alarmas y, en algunos casos, la implementación sin formación previa generó rechazo por parte del personal.
La lección clave es la colaboración continua entre desarrolladores y usuarios clínicos. Los algoritmos deben diseñarse con la participación de radiólogos y cirujanos desde la fase temprana para asegurar que las salidas sean clínicamente útiles y accionables.
Ejemplo ilustrativo (hipotético)
Imagine un hospital regional donde un sistema IA analiza TC abdominopélvicas en tiempo real y marca estudios con alta probabilidad de apendicitis. En el primer mes, la herramienta ayuda a priorizar tres estudios urgentes que tenían lecturas pendientes; en dos de ellos, la intervención precoz evitó complicaciones. Al mismo tiempo, se detecta un patrón de falsos positivos en pacientes con postoperatorios abdominales, lo que impulsa un ajuste de parámetros y la inclusión de un flag de antecedentes quirúrgicos en la entrada de datos. Esto muestra cómo la tecnología y el aprendizaje organizacional progresan juntos.
Futuro: hacia modelos más robustos y personalizados
El futuro de la IA en diagnóstico de apendicitis pasará por varias tendencias convergentes: modelos multimodales que integren imágenes, datos clínicos y laboratorio; aprendizaje federado que permita entrenar modelos con datos de múltiples centros sin compartir datos sensibles; y sistemas que no solo detecten apendicitis, sino que predigan riesgo de complicación y respuesta al tratamiento conservador. Además, la mejora en hardware permitirá procesar volúmenes 3D a velocidades mayores, haciendo viable la lectura asistida en tiempo real en centros con recursos limitados.
Otra tendencia es la creación de bancos de datos etiquetados y estandarizados accesibles para investigación, lo que acelerará el desarrollo y la validación de algoritmos robustos. La regulación también evolucionará hacia marcos que permitan actualizaciones continuas del modelo con monitoreo postcomercialización.
Investigación y colaboración
El progreso será más rápido cuando exista colaboración internacional: compartir protocolos de anotación, estándares de reporte y conjuntos de validación externos. También son necesarios ensayos clínicos que midan no solo métricas de rendimiento, sino impacto en resultados clínicos: reducción de perforaciones apendiculares, menos apendicectomías negativas, y mejor uso de recursos.
Recomendaciones prácticas para clínicos y administradores
A continuación una lista concisa de recomendaciones para equipos que consideran incorporar IA para diagnóstico de apendicitis desde TC:
- Evalúe evidencia científica y priorice herramientas con validación externa.
- Realice pilotos controlados y revise performance local antes de despliegue completo.
- Involucre a todos los actores: radiólogos, cirujanos, urgencias, TI y ética.
- Priorice modelos explicables y con interfaces intuitivas.
- Establezca protocolos de monitoreo continuo y métricas de impacto clínico.
- Garantice privacidad y conformidad regulatoria.
- Planee capacitación y soporte para adopción tecnológica.
Estas recomendaciones buscan minimizar riesgos y maximizar beneficios en la adopción responsable de tecnologías emergentes.
Resumen visual: ventaja vs. riesgo
| Ventajas | Riesgos |
|---|---|
| Mayor sensibilidad y especificidad potencial | Falsos positivos/negativos si no se valida adecuadamente |
| Reducción de tiempos y priorización de urgencias | Dependencia tecnológica y caída de habilidades humanas si se abusa |
| Estandarización en la interpretación | Sesgos en datos y desigualdades en poblaciones subrepresentadas |
| Apoyo educativo para residentes | Cuestiones regulatorias y de responsabilidad no resueltas |
Puntos clave para recordar
- La IA no reemplaza al clínico; lo asiste y amplifica su capacidad.
- La calidad de los datos y la validación externa son esenciales.
- Interpretabilidad, privacidad y regulación son tan importantes como la precisión técnica.
- La integración exitosa requiere planificación organizacional y formación continua.
Conclusión
La inteligencia artificial aplicada a tomografías para diagnosticar apendicitis ofrece una promesa real: mejorar la precisión diagnóstica, acelerar decisiones críticas y estandarizar procesos en entornos que a menudo están saturados; sin embargo, esa promesa solo se cumplirá si combinamos innovación tecnológica con rigor clínico, datos de calidad, validación externa, transparencia y una implementación responsable que proteja la privacidad y minimice sesgos. La adopción cuidadosa puede traducirse en mejores resultados para los pacientes —menos complicaciones, menos cirugías innecesarias y procesos más eficientes—, pero exige que los hospitales no vean la IA como una solución mágica, sino como una herramienta que debe integrarse con formación, gobernanza y evaluación continua. Si usted participa en la toma de decisiones, priorice pilotos bien diseñados, participación multidisciplinaria y métricas que vayan más allá de la simple AUC; solo así la inteligencia artificial podrá transformar de verdad el diagnóstico de apendicitis desde la TC, beneficiando a pacientes y equipos clínicos por igual.